现在的位置:主页 > 综合新闻 >
又一省份封杀未过评价产品,仿制药大洗牌,8万
【作者】网站采编【关键词】【摘要】全文2121字,阅读需6分钟 江苏省公共资源交易中心近日发出通告,对部分未通过一致性评价的药品做出暂停采购的处理。 《通告》显示,根据相关法规规定,同品种药品通稿仿制药质量
全文2121字,阅读需6分钟
江苏省公共资源交易中心近日发出通告,对部分未通过一致性评价的药品做出暂停采购的处理。
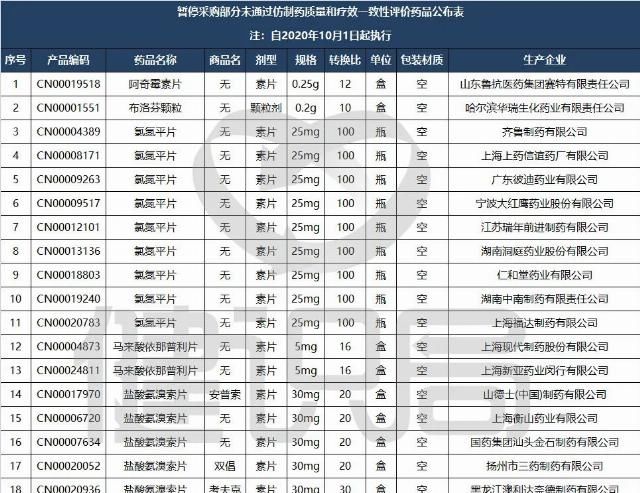
《通告》显示,根据相关法规规定,同品种药品通稿仿制药质量和疗效一致性评评价的生产企业达到3家以上的,不再选用未通过一致性评价的仿制药。
目前,江苏省公共资源交易中心已按相关程序对暂停采购部分未过评药品予以公布。
健识局梳理发现,此次暂停挂网的品种包括阿奇霉素片、布洛芬颗粒、氯氮平片、马来酸依那普利片、盐酸氨溴索片等5个品种,涉及19家药企,其中不乏知名企业,如上药信谊、齐鲁、山德士、现代制药等。
事实上,一致性评价是对仿制药产业影响最大的政策之一。这影响在于一旦药效无法达标就将面临暂停挂网并失去市场,因此各家药企都不可掉以轻心。
2018年11月,江苏省人民政府网曾转发新华日报文章《我省清理仿制药市场 不通过一致性评价将注销批文》在业界引起较大反响。
尽管该文章随即被网站删除,但江苏省政府转发此文也显示出了其清理仿制药的决心。
不仅仅是江苏,目前已有江西、浙江、广西、陕西、甘肃、辽宁、湖南、黑龙江、湖北等多省市发文明确落实暂停未通过一致性评价仿制药交易资格等事宜。
随着一致性评价政策的不断落地,不仅为国家药品集采提供了参考依据,也加速仿制药洗牌奠定了行业基础。
在产业升级、政策环境倒逼之下,业界估计,约8万批文将消失。无疑,这也将解决长期以来我国仿制药产业大而不强,低效重复问题严重。
恒瑞齐鲁天晴积极过评
仿制药进入优质低价产业竞争
按照国家医保局的计划,希望通过药品省级招标,逐渐将未通过一致性评价、临床疗效欠缺的品种淘汰出局。特别是,第三批国家集采8月底上海开标,拟中选产品191个,拟中选产品平均降价53%,最高降幅98%。
9月4日,北京市药品阳光采购平台发布通知称,第三批国家集采北京地区中选品种以及企业申报挂网,这也就意味着北京或将成为首个落地第三批药品集采的省市。
不过,业内普遍认为,其他省市跟进也仅仅是时间问题。
国家药品集采与一致性评价挂网相结合的政策组合拳,无疑启动了中国仿制药产业的淘汰赛。
有分析人士指出,今后仿制药行业会因大量未通过一致性评价产品出局,而市场份额走向集中,更为关键的是,药品集采会将仿制药的利润空间调整至合理区间。
从目前的市场趋势来看,就连恒瑞、齐鲁、正大天晴等大型药企都会受到市场及政策的影响,各家都在积极准备通过一致性评价而保住已获得市场优势。
据健识局不完全统计,截止目前约共有1022个品规通过一致性评价,其中104个品种已集齐三家以上过评,苯磺酸氨氯地平片、盐酸二甲双胍片、阿莫西林胶囊都是药企争夺的重点品种。
需要注意的是,虽然国家政策明确,通过一致性评价的品种在药品集采时将占据先机优势,但越来越多药企品种过评,市场的竞争也越发激烈。

健识局注意到,已有浙江、江苏、陕西、四川、湖南、山东、安徽等省市明确要求,承诺过评品种全国最低价联动。
随着仿制药进入到优质低价的市场竞争,相关药企的营销方式也必须进行调整。有分析人士指出,今后3-5年内,中国仿制药产业将得到根本性的变化,没有哪家企业和个人可以置身事外。
药品集采加速仿制药替代
跨国药企争夺院外及30%剩余市场
就在仿制药产业洗牌的同时,跨国药企的日子也不太好过。
在8月底的国家第三批药品集采中,安斯泰来、拜耳、百时美施贵宝、勃林格殷格翰、礼来、默沙东等多家跨国药企的品种,均由于报价等因素退出这次市场的争夺。
动辄每片仅几毛钱的仿制药价格,也让业界感叹,跨国药企曾经在中国“躺着赚钱”的日子宣告结束。业内普遍认为,国家药品集采加速仿制药替代,今后中国医药产业将进入仿制药巨头垄断的微利时代。
从各家跨国药企2020上半年财报中,健识局也发现辉瑞、拜耳与2019年同期相比,业绩下滑严重,主要原因是受全国药品集采的影响,而阿斯利康的逆势增长是对于中国市场逐步调整密不可分。
作为全球第二大医药市场,2018年,中国药品市场规模为1279亿美元,同比增长2.4%。预计中国市场未来5年将保持这种增长势头,年均增长5%。
文章来源:《药品评价》 网址: http://www.yppjzzs.cn/zonghexinwen/2020/0909/655.html

